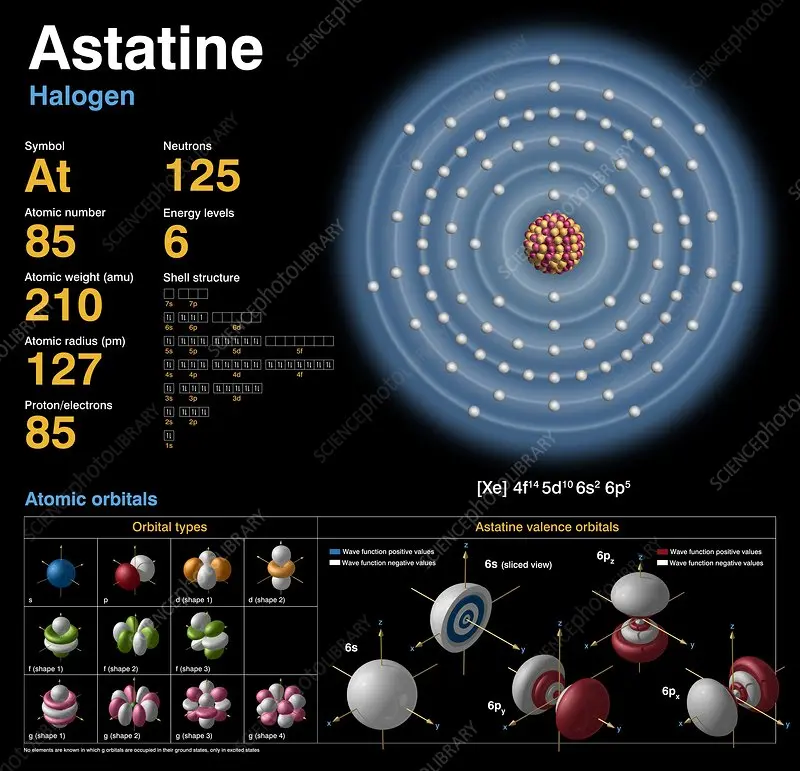
Астат: самый редкий и нестабильный галоген впервые получен в лаборатории
Финскими учеными получено ранее неизвестное ядро 190-астатина. Новый изотоп стал результатом эксперимента, проведенного в Лаборатории ускорителей Университета Ювяскюля, Финляндия. Ядро состоит из 85 протонов и 105 нейтронов и является самым легким изотопом астата, обнаруженным на сегодняшний день. Астат — быстроразлагающийся и очень редкий элемент. Во всей земной коре содержится не более одной столовой ложки астата.
Изотоп — разновидность атомного ядра с одинаковым числом протонов, но разным числом нейтронов. Число протонов определяет химический элемент, а число нейтронов влияет на его массу и стабильность. Например, водород имеет три изотопа: протий (1 протон), дейтерий (1 протон и 1 нейтрон) и тритий (1 протон и 2 нейтрона). Тритий — радиоактивный изотоп водорода, который распадается с периодом полураспада около 12 лет.
Эксперимент по получению нового изотопа астата был проведен с помощью ускорителя частиц — устройства, которое придает высокую скорость заряженным частицам, таким как протоны или ядра атомов. Затем эти частицы сталкиваются с другими атомами или ядрами, вызывая различные ядерные реакции. В данном случае ученые использовали пучок ядер стронция-84, которые бомбардировали мишень из серебра. В результате столкновения образовались новые ядра астата-190 и нейтроны. Эти ядра были отделены от других продуктов реакции с помощью специального детектора — рекойл-сепаратора RITU.
Зачем изучать астат? Астат — самый тяжелый из галогенов — группы элементов, к которой также относятся фтор, хлор, бром и йод. Галогены обладают высокой химической активностью и способностью образовывать соединения с большинством других элементов. Астат интересен тем, что он находится на границе между металлами и неметаллами и может проявлять как металлические, так и неметаллические свойства. Например, астат может быть полупроводником или даже металлом при высоких давлениях. Астат также может образовывать разные степени окисления: -1, +1, +3, +5 и +7. Степень окисления — число, которое показывает, сколько электронов передает или принимает атом при образовании химического соединения.
Изотоп — разновидность атомного ядра с одинаковым числом протонов, но разным числом нейтронов. Число протонов определяет химический элемент, а число нейтронов влияет на его массу и стабильность. Например, водород имеет три изотопа: протий (1 протон), дейтерий (1 протон и 1 нейтрон) и тритий (1 протон и 2 нейтрона). Тритий — радиоактивный изотоп водорода, который распадается с периодом полураспада около 12 лет.
Эксперимент по получению нового изотопа астата был проведен с помощью ускорителя частиц — устройства, которое придает высокую скорость заряженным частицам, таким как протоны или ядра атомов. Затем эти частицы сталкиваются с другими атомами или ядрами, вызывая различные ядерные реакции. В данном случае ученые использовали пучок ядер стронция-84, которые бомбардировали мишень из серебра. В результате столкновения образовались новые ядра астата-190 и нейтроны. Эти ядра были отделены от других продуктов реакции с помощью специального детектора — рекойл-сепаратора RITU.
Зачем изучать астат? Астат — самый тяжелый из галогенов — группы элементов, к которой также относятся фтор, хлор, бром и йод. Галогены обладают высокой химической активностью и способностью образовывать соединения с большинством других элементов. Астат интересен тем, что он находится на границе между металлами и неметаллами и может проявлять как металлические, так и неметаллические свойства. Например, астат может быть полупроводником или даже металлом при высоких давлениях. Астат также может образовывать разные степени окисления: -1, +1, +3, +5 и +7. Степень окисления — число, которое показывает, сколько электронов передает или принимает атом при образовании химического соединения.
Наши новостные каналы
Подписывайтесь и будьте в курсе свежих новостей и важнейших событиях дня.
Рекомендуем для вас

Ельцин не должен был победить: кого Горбачев хотел сделать президентом России?
Почему этот план с самого начала был обречен на поражение?...

Судьба имперских субмарин решена: почему они останутся на дне Крыма навсегда?
Как военные судна вообще оказались затоплены и кто мешал их изучению долгие десятилетия?...

Токийская декларация-1993: какую бомбу заложил Ельцин под Россию?
Эксперты говорят: российский президент хотел переиграть Токио, но в итоге дал японцам мощный рычаг воздействия на нашу страну...

140 стрел и пепел раскрыли тайну гибели самого загадочного города Руси, Гнездово
Город не зачах, не был расселен из-за политических разборок, его уничтожили быстро и жестоко...

Почему у самого большого железного метеорита на Земле вообще нет кратера?
Астрофизики говорят: метеорит Хоба в Намибии нарушает все правила природы вот уже 80 000 лет...

Стало известно о 9000-летней строительной технологии, которую почти невозможно повторить даже сейчас
Древним секретом активно интересуются сразу две ведущие промышленные организации в Израиле. Интересно, почему?...

Архив ФСБ раскрыл детали одной из самых дерзких диверсионных операций ВОВ
Биография Кирилла Орловского поражает. Две Звезды Героя, друг писателя Хемингуэя, ликвидатор нацистских палачей, председатель лучшего колхоза СССР...

Удар, который едва не расколол Луну пополам: кратер в 1/10 площади планеты оставил не просто астероид
Столкновение было настолько мощным, что на поверхность выбросило породы с глубины… почти 100 километров!...

Биоинженер провел 100 дней под водой. По его словам, это прибавило ему 10 лет жизни
Почему этот эксперимент вызвал массу критики? Кто победит, официальная теория или опытная практика?...

Правительство США рассекретило почти 200 файлов о неопознанных воздушных явлениях
Американские власти и Пентагон признаются: по большинству фактов нет однозначных решений. Почему?...

Выяснилось: как британская разведка создала миф о Распутине, чтобы потом его убить
Еще одна история о том, что Англия во всем времена была главным врагом России...

Иран «ставит на счетчик» мировой интернет: сможет ли Тегеран заставить Запад платить за кабели в Ормузе?
Как оказалось, нефть была только началом. Теперь Тегеран берет за горло западную цифровую экономику...